Nel campo della scienza dell’alimentazione si assiste ultimamente ad una notevole valorizzazione dell’importanza della funzione dei sali minerali che, in base al fabbisogno quotidiano, sono generalmente suddivisi in tre gruppi :
- Macrominerali, elementi il cui fabbisogno giornaliero è superiore ai 100 mg ( Ca, P, Na, K,Cl,Mg,S ).
- Microminerali, elementi il cui fabbisogno giornaliero è compreso tra valori inferiori a 1 mg e valori sino ai 100 mg ( Fe, Cu,Zn,Mn,I,Mo,Se,F,Br,Cr,Co,Si,B ).
- Oligoelementi , il cui reale fabbisogno non è stato ancora stabilito, ma sembra essere dell’ordine dei microgrammi ( As,Sn,Ni,Ge,V,W,).
Altri elementi vengono invece definiti come sostanze estranee e la loro presenza, al di là di certe quantità, è nociva per l’organismo ( Pb,As,Cd,Hg,Ba,Al,Li,Be,Ag,Au,Sb).
E’ importante sottolineare che i minerali sono definiti essenziali se:
- la loro carenza provoca un deficit funzionale.
- la loro somministrazione come supplementi è importante per lo sviluppo.
- i sintomi della loro carenza sono associati a una diminuita concentrazione nel sangue o in altri liquidi corporei.
IODIO
Tra i microminerali più importanti è certamente lo iodio, necessario alla produzione da parte della tiroide di due ormoni, la tiroxina e la triiodiotironina, che regolano diversi processi metabolici all’interno delle maggior parte delle cellule e svolgono un ruolo cruciale nelle prime fasi della crescita e nello sviluppo di vari organi, tra i quali il cervello. La conseguenza più conosciuta, anche se meno grave di altre, è il gozzo, ovvero l’ingrandimento della tiroide che può essere endemico in certe popolazioni.
Da analisi sulla popolazione italiana nei primi anni del duemila emerse che una parte non trascurabile ( il 10% ) soffriva di patologie legate a una non sufficiente assunzione di questo elemento con la dieta.
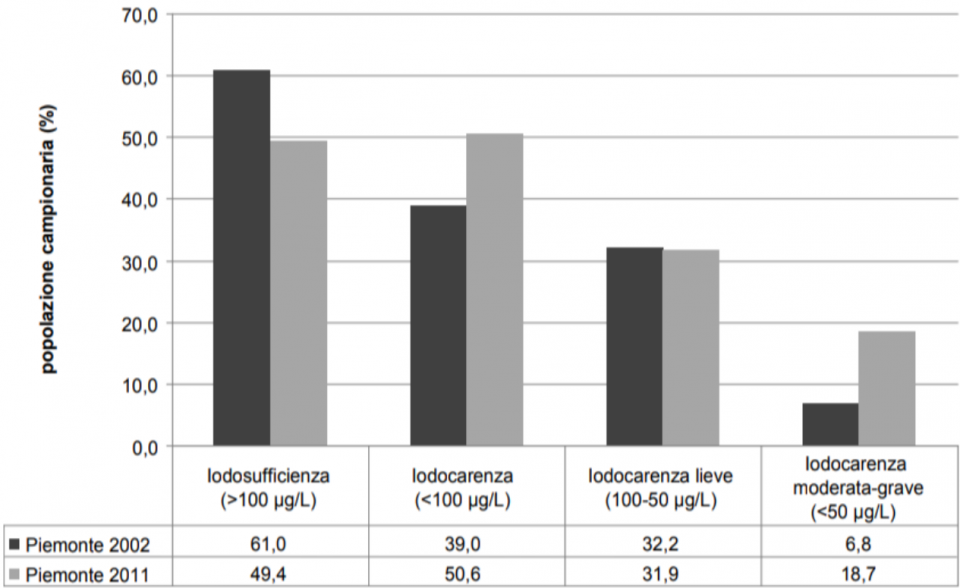
Con la legge L55/2005 lo Stato Italiano incentivò nella grande distribuzione la vendita di sale iodato e la sua messa a disposizione del cliente in ristoranti e mense aziendali. Tra il 2015 e il 2016 l’ISS ha promosso una indagine in tutta Italia, su 2500 bambini in età scolare volto a monitorare il loro stato nutrizionale iodico. Solo in quattro regioni ( Ligura, Toscana, Marche e Lazio ) si sono raggiunti i valori di iodosufficienza. Il Piemonte, in particolare, secondo l’Osservatorio Regionale “ vive ancora in uno stadio di iodio-carenza “ mentre “neppure la metà della popolazione piemontese utilizzi sale iodato ( 47,25 % ) specie nella città di Torino.
LUOGHI COMUNI
Qui vengono riportate alcune delle affermazioni che più frequentemente si incontrano in rete e che colpiscono l’immaginario del lettore ( è importante sottolineare il fatto che i siti da cui sono tratte non sono siti “neutri” ):
- Sale iodato definito come sale privato– in seguito a raffinazione – dello iodio naturale, addizionato poi con “iodio chimico” ( ? )
- Sul sale integrale: sale dal colore grigiastro, dall’aspetto grumoso e molto umido che offre minerali preziosi, tra cui lo iodio , oligoelemento essenziale che con la raffinazione del sale si perde, salvo poi ritrovarlo in quesi sali iodati in cui viene addizionato artificialmente
- Sul sale da cucina “sbiancato, privo di oligoelementi, spesso contiene additivi“
- Il nostro sale si forma dall´evaporazione naturale dell´acqua di mare. Durante il processo di trasformazione non viene sbiancato, nè raffinato artificialmente, e pertanto non subisce alcun trattamento chimico. Viene infine macinato e confezionato senza l´aggiunta di additivi antiagglomeranti.
- Il sale può essere usato come una vera e propria medicina... nei granuli bianchissimi che abbiamo sulla mensola, sbiancati e trattati non rimane più nulla degli 82 elementi terapeutici originari. Viene affermato che il sale grigio contiene 92 delle 93 tracce di minerali, che il sale dell’Himalaya ne contiene 84, che il sale rosso delle Hawaii 80.
La lettura degli articoli seguenti aiuta gli studenti a una rileggere in modo critico le informazioni precedentemente raccolte e fornisce suggerimenti per la progettazione di esperimenti rivolti a verificare alcune delle affermazioni ricorrenti.
http://bressanini-lescienze.blogautore.espresso.repubblica.it/2015/10/05/saleintegralissimo/
http://bressanini-lescienze.blogautore.espresso.repubblica.it/2015/11/09/grigiorosso-o-solo-sporco/
http://bressanini-lescienze.blogautore.espresso.repubblica.it/2015/12/09/sale-rosa-dellhimalaya-no-grazie/
http://bressanini-lescienze.blogautore.espresso.repubblica.it/2017/07/03/le-mille-bufale-del-sale-rosa-dellhimalaya/
PROGETTAZIONE
Si propone agli studenti di compilare il foglio di lavoro ( all.1 ) ricercando informazioni e dati relativamente ai seguenti punti:
- Composizione chimica media del residuo salino ottenibile per evaporazione dell’acqua di mare.
- Concentrazione media nelle acque marine dei microminerali / oligominerali su cui si focalizzeranno gli esperimenti.
- Concentrazione media nel sale/nei sali dei microminerali/ oligominerali su cui si focalizzeranno gli esperimenti.
- Consumo di sale suggerito dalla OMS.
- Fabbisogno di Ferro nella dieta giornaliera.
- Fabbisogno di Iodio nella dieta giornaliera.
Di seguito vengono elencate le esperienze che sono state suggerite dagli studenti che hanno contribuito alla elaborazione di questa esperienza: tale elenco potrà essere ovviamente arricchito nel tempo con altre proposte…
- Preparazione dei campioni di sale.
- Ricerca qualitativa dello iodio in diversi campioni di sale.
- Ricerca qualitativa del ferro in diversi campioni di sale.
- Determinazione iodimetrica dello iodato di potassio in un campione di sale iodato.
- Determinazione spettofotometrica del ferro in un campione di sale.
- Determinazione spettofotometrica del ferrocianuro in un campione di sale.
- Determinazione spettrofotometrica dello iodato in un campione di sale.
Le ultime tre esperienze non possono essere condotte con la attuale strumentazione dei nostri laboratori.
PREPARAZIONI DEI CAMPIONI
I sali utilizzati per le esperienze sono i seguenti:
- Sale integrale.
- Sale iodato.
- Salgemma.
- Sale grigio di Bretagna.
- Sale rosso delle Hawaii.
- Sale rosa dell’Himalaya.
- Sale nero di Cipro.
Prima di procedere alle analisi qualitative viene proposto agli studenti di verificare il fatto che la colorazione di alcuni sali è legata alla presenza di impurità, che nel caso dei sali marini sono in pratica “aggiunte” durante la lavorazione. Si procede quindi alla filtrazione di una certa quantità di ciascun sale. Il filtrato viene in parte conservato, per le analisi successive, e in parte sottoposto ad evaporazione. Il filtro viene anch’esso conservato. Ogni passaggio della preparazione va documentato con immagini ( a ogni gruppo di lavoro è fornito un tablet ) che serviranno poi a compilare il foglio di lavoro. – all.2
MATERIALE OCCORRENTE:
- -Strumentazione per la filtrazione: sostegni e imbuti per ogni campione di sale.
- Becher da 200 mL ( due per ogni campione di sale ).
- Bacchettine di vetro.
- Spruzzetta.
- Bilancia tecnica.
PROCEDIMENTO:
- Pesare circa 15 g di sale e discioglierlo in 50 mL di acqua.
- Mescolare sino a dissoluzione del campione.
- Preparare la strumentazione per la filtrazione e filtrare.
- Raccogliere parte del filtrato in una provetta, segnare sia sulla provetta che sul becher contenente il resto del filtrato la tipologia di sale utilizzato.
- Riporre la provetta in un portaprovette per le analisi successive.
Ripetere per ogni campione.
Il contenuto all’interno dei becher viene lasciato evaporare: il residuo è il sale di partenza, privato delle impurezze che lo rendevano eventualmente colorato. Il filtro viene rimosso e conservato.
Si compila il foglio di lavoro sia nella parte iconografica che in quella testuale.
RICERCA QUALITATIVA DEL FERRO
La ricerca del ferro viene compiuta, per ogni tipo di sale, sia su un campione “ex-novo” sia sul filtrato ottenuto nella fase precedente. Il campione “ex-novo” viene trattato con un attacco acido, simile a quello che prepara all’analisi dei vari gruppi analitici: non vengono quindi separate dalla frazione analitica per filtrazione le impurezze presenti e insolubili in acqua.
I reagenti utilizzati per mettere in evidenza le presenza del ferro sono quelli classici dell’analisi qualitativa: il tiocianato di potassio e il ferrocianuro di potassio.
Ogni passaggio della preparazione va documentato con immagini ( a ogni gruppo di lavoro è fornito un tablet ) che serviranno poi a compilare il foglio di lavoro – all.3
STRUMENTAZIONE:
- Centrifuga.
- Piastra riscaldante.
- Provette da centrifuga.
- Becher da 400 mL.
- Pipette monouso.
- Cartine indicatrici pH.
REAGENTI:
- HCl – 2N H314-331, P 305+351+338, 310, 410+403
- NH4Cl H 302, 309, P 305+351+338
- NaOH – 6M H 314 P 301+330+331, 305+351+338, 308+310
- KSCN – 1M H 332,312,302,402 P 302+352
- K4Fe (CN)6 – 0,1M H 412, P 273
Ecco qui le schede dell’esperienza Cum grano salis